Thérapie Fonctionnelle Cognitive de la lombalgie chronique non spécifique
| Auteur | Rubrique de cours | Relecteur | Responsable |
| Nicolas Adenis | Moyens Thérapeutiques | Bénédicte ANSEL | Jan-Hendrik Maitre |
Définition [1]
La Thérapie Fonctionnelle Cognitive (TFC) est une approche de gestion centrée sur le patient qui cible les croyances, les peurs et les comportements associés (mouvements, activités et mode de vie) de chaque individu souffrant de maux de dos persistants et handicapants.
Principes [1]
Cette thérapie conduit la personne à être consciente que la douleur n’est pas le reflet de dommages structurels – mais plutôt un processus où la personne est prise au piège dans un cercle vicieux de douleur, de détresse et de handicap. Ce cercle vicieux est alimenté par des systèmes de protections (système nerveux, système hypothalamo-hypophysio-surrénalien) hyperactifs influencés par une multitude de facteurs biopsychosociaux tels que la persistance de croyances négatives, de comportements mal adaptés et de facteurs issus de l’hygiène de vie.
Cette thérapie est intégrée à l’aide d’une approche de communication axée sur l’entretien motivationnel, où il identifie les divergences entre les croyances et les comportements et reconnaît que les solutions qui tiennent sur le long terme sont généralement trouvées par la personne elle-même. La TFC est fortement orientée sur le comportement et explore différentes options de mouvement en utilisant une rétroaction visuelle pour que les gens puissent rétablir leur schéma corporel et réapprendre les éléments de base du mouvement normal et détendu. Il donne à la personne le pouvoir de faire les choses elle-même qu’elle craint ou qu’elle évite, mais d’une manière graduelle et détendue. Cela les motive à s’engager dans l’exercice et la vie active en fonction de leurs préférences et leurs objectifs.
Contexte [2 – 4]
La lombalgie chronique non spécifique (LCNS) est une pathologie fréquente et souvent complexe à traiter, cela vient de son aspect multifactoriel. Des facteurs ont été identifiés dans la littérature mais ils ne peuvent pas être généralisés à tous les patients. Ces différents facteurs sont présents chez chaque patient à différents degrés et doivent être identifiés lors d’une évaluation méticuleuse et spécifique du patient lombalgique. La littérature décrit de nombreux facteurs dans différents domaines :
Facteurs anatomo-pathologiques : L’imagerie peut s’avérer nécessaire dans certains cas (drapeaux rouges, déficit neurologique). Cependant, les anomalies retrouvées au niveau des imageries sont mal corrélées avec les niveaux de douleurs et d’invalidité, et sont fréquemment retrouvés dans la population asymptomatique [5 ; 6]. Si la présence de dégénérescence avancée est associée au risque d’avoir une lombalgie, elle ne prédit pas une lombalgie à venir. En revanche, il existe des preuves que la description des éventuelles anomalies observées à l’imagerie (arthrose, discopathie, protrusion, fissure), sans évoquer la prévalence élevée de ces anomalies dans des populations asymptomatiques, peut avoir un réel effet Nocebo, qui favorise le catastrophisme, mais aussi la douleur et le recours aux soins médicaux [7 ; 8].
Facteurs physiques : Les niveaux et les schémas d’exposition à la charge spinale mécanique liés aux activités de la vie quotidienne, au travail et / ou au sport, impliquant un chargement lourd et / ou répété, une flexion et une torsion incommodes, sont connus pour être associés à la LCNS [9 ; 10]. Cependant, il s’agit là de facteurs contributifs potentiels, qui n’ont pas montré de lien de causalité, qui ne sont pas aussi important que le grand public le pense [11].
Facteurs neurophysiologiques : Il existe de plus en plus de données qui attestent le fait que des remaniements neurophysiologiques périphériques et centraux sont associés à la lombalgie persistante [12]. La LCNS apparaîtrait comme une image mixte reflétant la combinaison de mécanismes périphériques (bottum-up) et centraux (top-down). Elle a également été associée à des modifications cérébrales telles qu’une perte de matière grise, une augmentation de l’état cérébral au repos, des modifications du cortex sensorimoteur (altérations du schéma corporel) et une perte de l’inhibition de la douleur endogène [13 ; 14]. Ces facteurs peuvent contribuer à la sensibilisation des tissus, ainsi qu’à une modification du contrôle moteur et des perturbations du mouvement.
Facteurs cognitifs : Les croyances négatives, le catastrophisme et la peur du mouvement sont prédictifs de handicap et sont liés à la LCNS [15]. Ces croyances négatives peuvent tirer leur origine des professionnels de santé et avoir un impact dévastateur sur le pronostic de la lombalgie [16].
Facteurs psychologiques : Il existe des preuves de plus en plus nombreuses sur le fait que des facteurs tels que les troubles du sommeil, les niveaux de stress élevés et durables, l’humeur dépressive et l’anxiété sont de bons prédicteurs de la lombalgie [17]. Ces facteurs peuvent agir pour renforcer les mouvements inadaptés et les comportements liés au mode de vie, augmentant ainsi les niveaux de sensibilisation et d’incapacité [17]. Ils peuvent également conduire à un dérèglement de l’axe hypothalamo-hypophyso-surrénalien, altérant le traitement de la douleur centrale et la fonction immunitaire et neuro-endocrine, favorisant la sensibilisation centrale [18 ; 19].
Facteurs comportementaux
- Moteurs : La lombalgie est fréquemment associée à des comportements fonctionnels douloureux tels que des postures et des schémas de mouvement modifiés liés à des altérations du mouvement, du contrôle moteur ou du chargement de la colonne [20]. Des preuves croissantes suggèrent que ces comportements sont souvent mal adaptés et provocateurs en LCNS [20 ; 21]
- Communicationnels : Des comportements douloureux communicationnels (expression manifeste du visage et du corps de douleur) sont également considérés comme inadaptés dans la LCNS (en l’absence de pathologie) et dans certains cas de lombalgie aiguë non traumatique [22]. Ils sont corrélés avec la douleur catastrophique, offrant des opportunités pour cibler gestion comportementale [23].
- Lié à l’activité : Certains patients présentent un déconditionnement lié à des stratégies d’évitement et des modes de vie sédentaires qui peuvent renforcer des comportements fonctionnels mal adaptés associés au trouble. A l’inverse, d’autres patients présentent un sur conditionnement lié à des stratégies de confrontation [24 ; 25].
Facteurs sociaux : Ils peuvent inclure les facteurs liés au travail (stress, insatisfaction, absentéisme) [26], à la famille, à la culture, et au statut socio-économique [12]. Bien que souvent non modifiables, ils peuvent influer sur les croyances liées à la douleur, la capacité d’adaptation et la charge de stress.
Facteurs liés au mode de vie : Ces facteurs sont modifiables et peuvent contribuer à la fois aux mécanismes périphériques et centraux. Il existe également des preuves de l’importance des comorbidités liées à la santé et à la douleur associées à la lombalgie et de leur rôle pour influer sur les niveaux d’incapacité, l’état de santé général et la chronicité [27].
Facteurs individuels : tels que les objectifs du patient, les préférences, les connaissances en matière de santé, les niveaux d’acceptation, les attentes et la volonté de changement [28-29].
Facteurs génétiques : Il existe de la littérature croissante pour soutenir le rôle important qu’ont les facteurs génétiques sur la patho-anatomie (dégénérescence discale, protrusion, etc.) et sur la vulnérabilité à la douleur [30 ; 31].
Ces facteurs pouvant être indépendants ou interconnectés, il semble important de connaître les liens entre eux pour optimiser le traitement.
Évaluation [32]
Entretien individuel : Il s’agit d’un entretien individuel centré sur le patient qui implique d’entendre toute l’histoire du patient concernant sa douleur, la zone et la nature de sa douleur, le comportement de la douleur (les mouvements et activités qui améliorent / aggravent), les principales déficiences fonctionnelles (posture, mouvement et activités qu’ils ne peuvent plus faire à cause de leur douleur) ainsi que leurs comportements de santé (activité physique, habitudes de vie) et leurs schémas de sommeil. Les patients sont également interrogés sur leurs niveaux de peur de la douleur, l’évitement d’activité, sur leur travail et leurs engagements sociaux. Leur degré de focalisation sur la douleur, leur stratégie d’adaptation, leur réponse au stress et leur relation vis-à-vis de la douleur sont alors établis, ainsi que toute histoire d’anxiété ou de dépression. Finalement, leurs croyances et leurs objectifs concernant la gestion de leur trouble sont également vérifiés.
L’examen physique : Il comprend l’analyse des principales tâches fonctionnelles (postures, mouvements et activités de la colonne vertébrale) considérées comme douloureuses, craintes et / ou évitées au cours de l’entretien. Au cours de cet examen, les stratégies comportementales sont soigneusement observées, notamment la présence de comportements sécuritaires moteurs et communicationnels. Lorsque ces tâches impliquent des activités de chargement, le conditionnement physique (force et endurance) est également pris en compte. La palpation est effectuée au cours de ces tâches pour évaluer les niveaux de sensibilité des tissus, la protection des muscles du tronc et les schémas respiratoires. Les individus sont interrogés sur leurs croyances, leurs émotions, leurs perceptions corporelles et leurs réactions à la douleur lors de l’exécution de ces tâches. Ces observations constituent ensuite la base d’une série d’expériences comportementales guidées cherchant explicitement à réduire les réactions sympathiques et les comportements moteurs et communicationnels de sécurité. Ces expérimentations serviront d’une part à déconstruire les croyances antérieures du patient, et d’autre part d’exercices d’exposition graduelle.
Triage [2 ; 34]
La première démarche consiste à écarter les drapeaux rouges qui éliminent les lombalgies spécifiques (1-2% des lombalgies) : celles qui sont dues à une pathologie sérieuse systémique (tumeur, infection, syndrome inflammatoire systémique, fracture, etc.).
La seconde démarche consiste à écarter toute pathologie spécifique associée à un déficit neurologique (5-10% des lombalgies) : cela peut comprendre toute compression radiculaire (disque, sténose latérale), canal lombaire étroit et spondylolisthésis symptomatique.
Les 85 à 90% restants des personnes atteintes de lombalgie ne présentent aucune pathologie spécifique (lombalgie non spécifique) et présentent leurs propres facteurs contributifs uniques dans les domaines cognitifs, psychosociaux, physiques et du mode de vie. Ces patients peuvent être triés en fonction de :
- la temporalité de la lombalgie : aigüe, subaigüe, persistante ou récurrente ;
- les facteurs psychosociaux évaluant le risque de chronicisation (faible, moyen ou élevé) qui peuvent être évalués à l’aide du questionnaire Start Back ou du questionnaire d’Orebro.
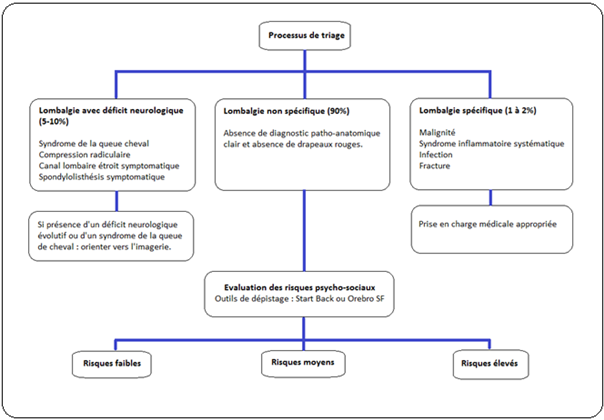 Triage (adapté de Lin et O’Sullivan, 2014)
Triage (adapté de Lin et O’Sullivan, 2014)
Raisonnement clinique [33]
Plutôt que de représenter un système de sous-groupe rigide, la TFC fournit un cadre souple, fournissant une orientation pour l’évaluation clinique et la gestion centrée sur la personne. En effet, bon nombre de ces facteurs coexistent, ne s’excluent pas mutuellement et ont le potentiel de sensibiliser à la fois périphériquement et centralement les structures spinales, renforçant les comportements d’invalidité en présence ou en l’absence de pathologie spinale. Certains de ces facteurs sont modifiables alors que d’autres ne le sont pas. La prise en compte de la contribution relative des différents facteurs est importante pour une gestion ciblée (dans certains cas multidisciplinaire) ainsi que pour un pronostic réaliste et l’établissement d’objectifs.
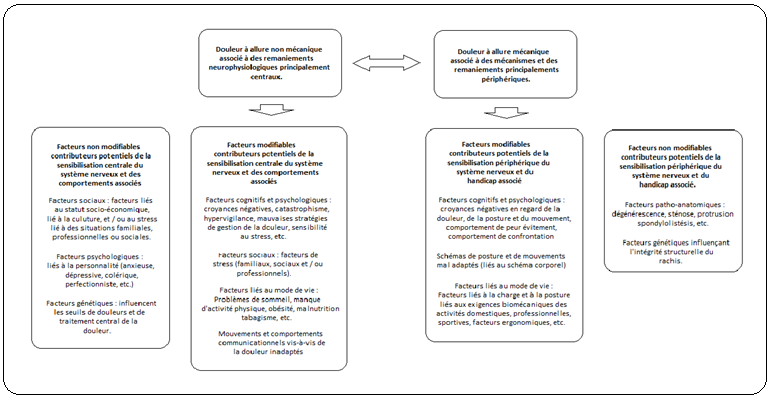 Raisonnement clinique (adapté de O’Sullivan et al, 2015)
Raisonnement clinique (adapté de O’Sullivan et al, 2015)
Traitement [30 ; 5]
Les patients reçoivent une intervention individualisée visant à modifier les comportements cognitifs, fonctionnels et comportement de santé (style de vie), considérés comme participant à la persistance des douleurs et de l’incapacité. Ce traitement comprend 3 composantes : Faire sens à la douleur, l’exposition avec contrôle et le changement des facteurs liés à l’hygiène de vie. Ces composantes peuvent se chevaucher au cours du traitement.
Faire sens à la douleur
Faire sens à la douleur est un processus réflexif ou le thérapeute rassure le patient sur la nature bénigne (exclusion de redflags, de pathologie spécifique ou neurologique) mais handicapante de son affection. Le thérapeute explique comment les facteurs contextuels, les croyances négatives au sujet de la douleur et les réponses émotionnelles et comportementales inadaptées entretiennent un cercle vicieux de sensibilisation centrale, de détresse et de handicap. Le thérapeute explique ensuite comment ce cercle vicieux constitue un obstacle pour accomplir les objectifs qui ont du sens pour eux (réduction de la douleur, réduction de la gêne, accomplissement d’activité qui ont du sens pour eux). Cette information est rédigée sur papier et discutée d’une manière réflexive et collaborative. Les patients sont ensuite invités à réfléchir sur les moyens pour briser ce cercle vicieux dans le but d’atteindre leurs objectifs qui ont du sens pour eux. À travers ce processus, des stratégies claires et réalistes pour le changement de comportements dirigés vers leurs objectifs personnels sont identifiées. Des ressources en lignes et des histoires de patients sont également fournis pour faciliter le processus.
Exposition avec contrôle
L’exposition avec contrôle est un processus de changement de comportement par apprentissage par l’expérience, dans lequel le patient est amené à s’exposer à des mouvements douloureux, redoutés ou évités, en se focalisant sur le contrôle des comportements de protection via la respiration diaphragmatique détendue, la relaxation corporelle, la prise de conscience et le contrôle. Le but étant d’amener graduellement le patient à retourner faire les activités fonctionnelles qui ont du sens pour lui, sans escalade des niveaux de douleur et de détresse. Ce processus permet de violer les attentes du patient, offrant un outil puissant de déséducation, d’éducation et de rééducation. Une fois les stratégies de contrôle des comportements de protection acquis, le patient est immédiatement encouragé à intégrer graduellement ces nouveaux comportements dans ses AVQ, sur la base des objectifs personnels et des niveaux de sensibilité du patient. Ceci, afin de généraliser l’apprentissage et construire de l’auto-efficacité dans ces tâches. Le patient est encouragé à reprendre une activité physique selon ses préférences, et en fonction de ses niveaux de sensibilité et de ses capacités d’autorégulation, le patient est amené à s’y exposer graduellement d’une manière temps-contingent. Les patients sont vus initialement 1 fois par semaine les 2-3 premières séances, puis les séances sont étendues toutes les 2-3 semaines afin de construire de la confiance pour s’autogérer sur une période de 12 semaines. Des stratégies sont proposées en cas de poussées douloureuses, et des séances additionnelles peuvent être proposées au-delà de la période 12 semaines si la douleur devient de nouveau incontrôlable, stressante ou handicapante. Plutôt que prescriptive, l’éducation est réflective : le patient est encouragé à trouver de nouvelles stratégies pour contrôler la douleur, et performer les activités qui lui font sens avec confiance, sans réactions de surprotection. Tous les patients sont informés des effets bénéfiques de l’activité physique sur la santé en rapport avec leur histoire (ex : humeur, stress, sommeil, etc.).
Hygiène de vie
Parallèlement aux composantes précédentes, les facteurs d’hygiène de vie pouvant contribuer à la sensibilisation des systèmes de protection homéostatiques, tels que le manque d’activité physique, la sédentarité ou le manque de sommeil, sont discutés avec le patient dans un style motivationnel.
 Thérapie Fonctionnelle Cognitive (adapté de O’Sullivan et al, 2015)
Thérapie Fonctionnelle Cognitive (adapté de O’Sullivan et al, 2015)
Conclusion [4]
La Thérapie Fonctionnelle Cognitive est donc une approche évaluative, relationnelle et thérapeutique centrée sur le patient. Elle vise, à travers un raisonnement clinique souple basé sur un cadre biopsychosocial, à amener le patient à modifier les facteurs considérés comme participant à la provocation et / ou la persistance de ses douleurs, de sa détresse et de son handicap. La TFC fournit au patient une compréhension multidimentionnelle de sa douleur dans le contexte de leur propre histoire. Les stratégies de contrôle de la douleur et des comportements de sécurités sont utilisés pour permettre au patient de revenir aux activités saines et / ou qui ont du sens pour elles. L’objectif de ce processus est de construire de l’auto-efficacité pour briser ce cercle vicieux de détresse, de douleur et d’invalidité.
Bibliographie
[1] https://bodyinmind.org/classification-based-cognitive-functional-therapy-for-back-pain/
[2] O’Sullivan P., Dankaerts W., O’Sullivan K., et Fersum K. Multidimensional approach for the targeted management of low back pain. Lumbar spine, chapter 3, 465-469.
[3] O’Sullivan P.B. (2012). It‟s time for change with the management of non-specific chronic low back pain. British Journal of Sports Medicine, 46(4), 224-227.
[4] O’Sullivan P.B., Caneiro J.P., O’Keeffe M., et al. (2018). Cognitive Functional Therapy : An integrated Behavioral Approach for the Targeted Management of disabling Low Back Pain. Physical Therapy, 98(5), 408-423.
[5] Brinjikji W., Luetmer P.H., Comstock B., et al. (2015). Systematic literature review of imaging features of spinal degeneration in asymptomatic populations. Journal of Neuroradiology, 36, 811-816.
[6] Carragee E.J., Alamin T.F., Miller J.L., et al. (2005). Discographic, MRI and psychosocial determinants of low back pain disability and remission: a prospective study in subjects with benign persistent back pain. Spine Journal, 5 : 24 – 35.
[7] Barker K.L., Reid M., Minns Lowe C.J. (2009). Divided by a lack of common language? A qualitative study exploring the use of language by health professionals treating back pain. BMC Musculoskelet Disord, 10, 123.
[8] Deyo R.A. (2013). Real help and redherrings in spinal imaging. The New England Journal of Medicine, 368: 1056-1058.
[9] Bakker E., Verhagen A., Van Trijfell E., Lucas C., et al. (2009). Spinal mechanical load as a risk factor for low back pain. Spine (Phila pa 1976), 34, 291-293.
[10] Coenen P., Gouttebarg V., Van Der Burght., et al (2014). The effect of lifting during work on low back pain : a health impact assessment based on meta-analysis. Occupational and Environmental Medicine, 71, 871-877.
[11] Roffey D.M., Wai E.K., Bishop P., Kwon B.K., et al. (2010). Causal assessment of worplace manual handling or assisting patients and low back pain : results of a systematic review. Spine Journal, 10(7), 639-651.
[12] Woolf C.J. (2010). Central sensitization: Implications for the diagnosis and treatment of pain. Pain, 152 : S2 – 15.
[13] Wand B., Parkitny L., O’Connell N., et al. (2011). Cortical changes in chronic low back pain: current state of the art and implications for clinical practice. Manual Therapy, 16 : 15 – 20.
[14] Moseley G.L. (2008). Pain, brain imaging and physiotherapy–opportunity is knocking. Manual Therapy, 13 : 475 – 7.
[15] Sullivan M., Thibault P., Andrikonyte J., et al. (2009). Psychological influences on repetition-induced summation of activity-related pain in patients with chronic low back pain. Pain , 141, 70 – 8 .
[16] Darlow B., Fullen B.M., Dean S., et al. (2012). The association between health care professional attitudes and beliefs and the attitudes and beliefs, clinical management, and outcomes of patients with low back pain: a systematic review. The European Journal of Pain, 16, 3 – 17.
[17] Gatchel R.J., Peng Y.B., Peters M.L., Fuchs P.N., Turk D.C. (2007). The biopsychosocial approach to chronic pain: scientific advances and future directions. Psychological Bulletin, 133: 581-624.
[18] Campbell C.M., Edwards R.R. (2009). Mind-body interactions in pain: the neurophysiology of anxious and catastrophic pain-related thoughts. Translation Research, 153 : 97 – 101.
[19] Ren K., Dubner R. (2010). Interactions between the immune and nervous systems in pain. Nat Med, 16 : 1267 – 76.
[20] Dankaerts W., O’ Sullivan P. , Burnett A., et al. (2009). Discriminating healthy controls and two clinical subgroups of nonspecifi c chronic low back pain patients using trunk muscle activation and lumbosacral kinematics of postures and movements: a statistical classification model. Spine, 34 : 1610 – 18 .
[21] O’ Sullivan P. (2005). Diagnosis and classification of chronic low back pain disorders: maladaptive movement and motor control impairments as underlying mechanism. Manual Therapy, 10 : 242 – 55.
[22] Koho P., Aho S., Watson P., et al. (2001). Assessment of chronic pain behaviour: reliability of the method and its relationship with perceived disability, physical impairment and function. Journal of Rehabilitation Medicine, 33 : 128 – 32.
[23] Martel M., Thibault P., Sullivan M. (2010). The persistence of pain behaviors in patients with chronic back pain is independent of pain and psychological factors. Pain, 151 : 330 – 6.
[24] Vlaeyen J., Linton S. (2012). Fear-avoidance model of chronic musculoskeletal pain: 12 years on. Pain, 153 : 1144 – 7.
[25] Smeets R.J., Wittink H., Hidding A., et al. (2006). Do patients with chronic low back pain have a lower level of aerobic fi tness than healthy controls?: are pain, disability, fear of injury, working status, or level of leisure time activity associated with the difference in aerobic fitness level? Spine, 31 : 90 – 7.
[26] Shaw W.S., Van der Windt D.A., Main C.J., et al. (2009). Early patient screening and intervention to address individual-level occupational factors (“blue fl ags”) in back disability. Journal of Occupational Rehabilitation, 19 : 64 – 80.
[27] Bjorck-van Dijken C., Fjellman Wiklund A., Hildingsson C. (2008). Low back pain, lifestyle factors and physical activity: a population-based study . Journal of Rehabilitation Medicine, 40 : 864 – 9.
[28] Hayes C., Hodson F.J. (2011). A whole-person model of care for persistent pain: from conceptual framework to practical application . Pain Medicine, 12 : 1738 – 49.
[29] Iles R.A., Davidson M., Taylor N.F., et al. (2009). Systematic review of the ability of recovery expectations to predict outcomes in non-chronic non-specific low back pain. Journal of Occupational Rehabilitation, 19 : 25 – 40.
[30] Battié M.C., Videman T., Parent E. (2004). Lumbar disc degeneration: epidemiology and genetic influences. Spine, 29 : 2679 – 90.
[31] Battie M.C., Videman T., Kaprio J., et al. (2009). The Twin Spine Study: contributions to a changing view of disc degeneration, Spine Journal, 9, 47-59.
[32] O’Keeffe M., Purtill H., Kennedy N., et al. (2015). Individualised cognitive functional therapy compared with a combined exercise and pain education class for patients with non-specific chronic low back pain : study protocol for a multicentre randomized controlled trial. British Medial Journal Open, 5(6).
[33] O’Sullivan P.B., et Lin I. (2014). Acute low back pain. Beyond drug therapies. Pain Management Today, 1(1), 8-13
[34] Vibe Fersum K., O‟Sullivan P., Skouen J.S., et al. (2013). Efficacy of classification-based cognitive functional therapy in patients with non-specific chronic low back pain: A randomized controlled trial. European journal of pain, 17(6), 916-928.

Laisser un commentaire